ページ内リンク
ブラインは満遍なく(P54~P56)
ブラインは、『初級 冷凍受験テキスト:日本冷凍空調学会』<8次:P54~P56>と、3頁に渡る。ポツポツ・ポツリと出題される、そして、満遍なくいろいろな問題があるので少々厄介かもしれない。
8次改訂版(2019(R01)年11月30日発行)は、全般的に内容が見直されており、自然冷媒の二酸化炭素については7行を割いて追加された。
ブラインとはP54
ブラインというのは、冷凍冷蔵庫とか、食品ケースとか、大型室内空調機などの蒸発器で冷却され循環して物を冷やすための媒体で、冷水とか、車で言えば不凍液のようなものです。
・ブラインは、一般に、凍結点が0℃以下の液体である。 by echo 
【◯】 凍結点とは、物質に含まれる水が凍り始める温度です。ですから、凍結点が0℃以下というのは当然?この凍結点は、溶解する種類や濃度で変わります。
・「塩水」の意味をもつ「ブライン」は「二次冷媒」とも呼ばれ、「潜熱」を利用して被冷却物を冷却する熱媒体である。 by echo 
【×】 ぁ~、「顕熱」です。テキスト<8次:P54 17行~>「潜熱」では、液体が蒸発や凝縮することになります。理科の実験での想い出、塩を水に入れると0℃以下になっても氷りませんでした。
・ブラインは、一般に凍結点が0℃以下の液体で、それの顕熱を利用してものを冷却する媒体のことである。 H15/04 
【◯】 凍結点とはブラインが凍りはじめる温度で、塩化カルシウムブライン(濃度29.9%で-55℃)、塩化ナトリウムブライン(食塩水)は最低で-21℃
である。テキスト<8次:P55 4行目~真ん中辺り>(要は、冷凍庫の魚などをコチコチに凍らせるための冷たいブラインが、先に凍結してしまったらお話にならない。)
顕熱:物体(この場合ブライン)の状態変化なしに温度のみを変化させる熱。
【8次改訂版について】 ← 読まなくていいよ、ま、 時間があったらどうぞ。
【8次改訂版における 顕熱
について】
「ブラインは顕熱のみ」という表記は消えている。二酸化炭素を二次冷媒としてアンモニア冷凍機と組み合わせ、顕熱と潜熱の両方を利用して効率よく冷凍、冷却を行えると記されている。ここで「二次冷媒」ブラインと同様の意味であろう。
7次では、「二次冷媒(ブライン)」と記されていたが、8次では、はてな?発行後の正誤表により (ブライン)
が消されてしまった。理由は不明。
テキスト<8次:P54 (4.5 ブライン)>の冒頭には、 ブラインは二次冷媒ともよばれる.
と記されているのだが…、はてな?
無機ブラインP54,P55
次の2つの種類と特徴を覚えましょ。テキスト<8次:P54 21行~>
- 塩化カルシウムブライン(塩化カルシウム水溶液)
製氷、冷凍、冷蔵、一般工業用 - 塩化ナトリウムブライン(塩化ナトリウム水溶液、食塩水)
食品に直接触れる場合に用いられる
無機ブラインの特徴
- 金属への腐食性が強い。(腐食抑制剤を添加する)
- 空気に触れると空気中の酸素が溶け込み金属の腐食が進む。
・塩化ナトリウムブラインは、食品に直接接触する場合に使用することがあるが、金属に対する腐食性が有機ブラインよりも強い。 H20/04 
【◯】 塩化ナトリウムは無機ブラインで、塩水のこと。
塩水をイメージすればなんとなく解ける問題。食品云々は<8次:P54の下から4行目、有機との腐食に関しては<8次:P55下から5行目~>一読熟読。頑張ろう。
・塩化カルシウムブラインは、金属に対する腐食性が大きいので、腐食抑制剤を加えるとよい。 H16/04 
【◯】 塩化カルシウムブライン
は 塩化ナトリウムブライン
同様「無機ブライン」である。腐食に関しては<8次:P54の下から3行目>、無機ブラインは腐食性が強いので腐食抑制剤が必要になる。
とにかくブラインは水質管理が重要、配管が腐食してしまわないように。
・ブラインは空気とできるだけ接触しないように扱われる。それは、窒素が溶け込むと腐食性が促進され、また水分が凝縮して取り込まれると濃度が低下するためである。 H27/04 
【×】 窒素ではなく、酸素。テキスト<8次:P54の下から2行目> よく読まないとヤラれてくやし涙になるかも…。
水分に関して(正しい)は、テキスト(P52)を一読しておかないと自信持てないかも。 ← 8次改訂版では 使用中に空気中の水分を凝縮させて取り込み,ブラインの濃度が下がるので,濃度の調整が必要である.<略>
この辺りの部分がゴッソリ削除されてしまった。理由は不明。
・無機ブラインは、できるだけ空気と接触しないように扱う。それは、酸素が溶け込むと腐食性が促進され、また水分が凝縮して取り込まれると濃度が低下するためである。 R04/04 
【◯】 テキスト<8次:P54の下~P55 図4.2> 図4.2から濃度が低下すると、温度が高く(0℃に近い方)ても凍結するようになる。
凍結温度(共晶点)P55
テキストは<8次:P55 4行~15行目>
- 塩化カルシウムブライン
凍結点:-55℃(濃度30mass%)
実用温度:-40℃くらい
- 塩化ナトリウムブライン
凍結点:-21℃
実用温度:-15℃まで
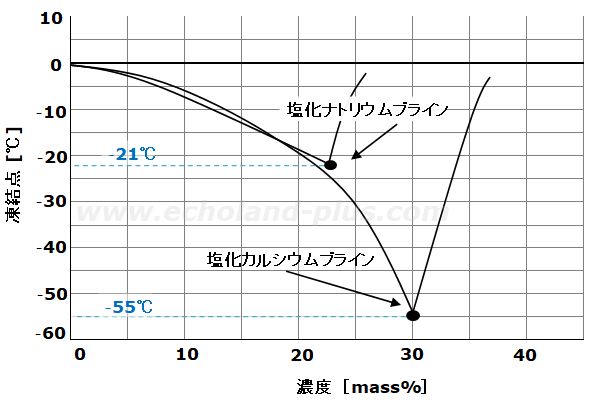
ブラインの凍結点イメージ図
(グラフ曲線はイメージですので、正確な数値は読み取りできません。)
・塩化カルシウムブラインの凍結点(共晶点)は、塩化ナトリウムの凍結点よりも低い。 H17/04 
【◯】 共晶点とは最低の凍結点のことで、塩化カルシウムブラインは-55℃、塩化ナトリウム(食塩)ブラインは-21℃、テキスト<8次:P55 6行目~>
「塩(ナトリウム)よりカルシウムの方が、やっぱし、強力で低いね」見たいな感じで覚えましたょ。
・塩化カルシウムブラインの共晶点は-55℃であるが、実用上使える下限温度は-40℃である。 H12/04 
【◯】 共晶点とは最低の凍結点のことで、塩化カルシウムブラインは-55℃くらい、塩化ナトリウム(食塩)ブラインは-21℃である。テキスト<8次:P55 6行目~>
─── 参考 ─── ← クリック
何事も考え過ぎはいけないのだが…、塩化カルシウムブラインは実用上の下限使用温度は-40℃くらいである。 くらい
は、テキストに記されている。でも、平成12年頃のテキスト(たぶん第3次改訂版)は定かではない。(問題が古すぎるかな。ま、参考程度にしといてちょうだい。)
・塩化カルシウムブラインの凍結温度は、濃度が0mass%から共晶点の濃度までは塩化カルシウム濃度の増加に伴って低下し、最低の凍結温度は-40℃である。 R03/04 
【×】 -40℃は塩化カルシウムの実用温度ですね。最低の凍結温度は-55℃です。テキスト<8次:P55 6行目~>
二酸化炭素P55
テキスト8次改訂版から、ブラインに二酸化炭素が登場した。テキスト<8次:P55 17行目~> 地球環境の観点からフロンから自然冷媒のアンモニアが見直されてきて、アンモニア冷媒の危険性に配慮できる二酸化炭素を二次冷媒とした間接冷却式設備が普及してきたようです。
・二酸化炭素は、アンモニア冷凍機などと組み合わせた冷凍・冷却装置の二次冷媒(ブライン)としても使われている。 R03/04 
【◯】 二酸化炭素二次冷媒(ブライン)は、近年普及しているのでテキストに追加されたのでしょう。この下に、概略図を載せておきましょう。
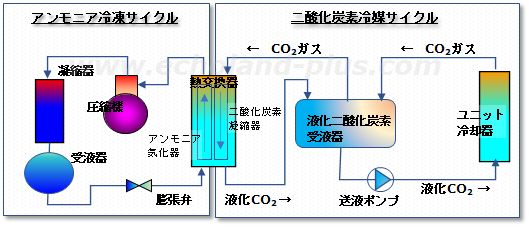
"アンモニア/二酸化炭素 二元式冷凍機" 二次サイクル概略図
参考:あいち産業科学技術総合センター
・二酸化炭素を二次冷媒として使用するシステムは、二次サイクルにおいて圧縮機を必要とせず、重力による自然循環または送液ポンプによる循環により、顕熱と潜熱の両方を利用して効率のよい冷凍・冷却を行うことができる。 by echo 
【◯】 塩化カルシウムブラインや塩化ナトリウムブラインは「顕熱」のみで冷却していたが、この二次サイクルシステムでは「液化二酸化炭素」が気化し「潜熱」の出入りも加わって冷却効率がより良くなる。(概略サイクル図参照)テキストは<8次:P55 19行~>
有機ブラインP55,P56
テキストは<8次:P55 23行~P56>
・有機ブラインの溶質には、エチレングリコール系やプロピレングリコール系のほかに、塩化カルシウムや塩化ナトリウムなどがある。 R02/04 
【×】 (><;) 塩化カルシウムや塩化ナトリウム
は、無機ブラインでしゅ。
特徴
- エチレングリコールブライン及びプロピレングリコールブライン共に、凍結点:-50℃(濃度60mass%)実用温度:-30℃くらい
- 腐食抑制剤を添加したブラインは金属を腐食しない。
- エチレングリコールは生体内で代謝すると有毒化する。
- プロピレングリコールは毒性がほとんどない。
用途
- エチレングリコール
冷却用ブライン、水冷エンジン用不凍液など - プロピレングリコール
冷却用ブライン、食品、飲料、医薬品、化粧品など
・腐食抑制剤を添加した有機ブラインは、無機ブライン同様に、金属を腐食するので注意が必要である。 by echo 
【×】 腐食抑制剤を添加した有機ブラインは、無機ブラインと異なりに、金属を腐食しない。テキスト<8次:P55 25行~>
・エチレングリコールブラインおよびプロピレングリコールブラインは、共に凍結点は-50℃(濃度60mass%)、実用温度は-30℃くらいである。 by echo 
【◯】 両方とも凍結点と実用温度は同じなので覚えやすいですね。テキスト<8次:P55 最終行>
21/12/25 23/02/23
『初級 冷凍受験テキスト』8次改訂版へ適応。(21(R03)/12/25)
修正・訂正箇所履歴
【2021(R03)/12/25 新設】
- -
-- コラム --
【参考文献】
- 初級 受検テキスト(SIによる初級受検テキスト):日本冷凍空調学会
- 上級 受検テキスト(SIによる上級受検テキスト):日本冷凍空調学会
- 冷凍機械責任者(1・2・3冷)試験問題と解答例(13):日本冷凍空調学会
- 第3種冷凍機械責任者試験模範解答集 :電気書院
- 第1・2種冷凍機械責任者試験模範解答集 :電気書院